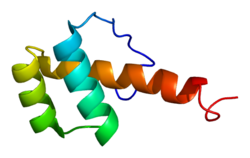
Гусикоидный белок - Goosecoid protein
Гоускоид протеин гомеобокс это белок что у людей кодируется GSC ген.[5][6]Этот ген кодирует члена подсемейства бикоидов из семейства парных (PRD) гомеобоксов белков. Кодируемый белок действует как фактор транскрипции и может быть ауторегуляторным. Подобный белок у мышей играет роль в развитии черепно-лицевой и грудной клетки во время эмбриогенеза.[6]
Серп Коллера является первым, экспрессирующим ген гомеобокса цыплят мурашки по коже (GSC).[7]
Функция
Ген GSC определяет спецификацию судьбы клеток нервного гребня и вносит вклад в формирование дорсально-вентрального паттерна. Чрезмерная активация в Xenopus способствует дорсо-передней миграции и дорсализации мезодермальный ткань клеток вместе с BMP-4.[8] И наоборот, анализ потери функций косвенно предотвратил образование головы в Xenopus [9] и дефекты головы у рыбок данио.[10] Хотя нокаут-исследования на мышах показали, что ген GSC не требуется для гаструляции, но все же происходит сокращение основания черепа. Мутация в гене GSC в Дрозофила смертельно.[11]
Ген Gsc способствует формированию Организатора Спеманна. Этот органайзер не позволяет БМП-4 вызывать эктодерма в будущем область головы эмбриона станет эпидермисом; вместо этого он позволяет будущей области головы образовывать нервные складки, которые в конечном итоге превратятся в головной и спинной мозг. Для нормального переднего развития организатор Спеманна не может экспрессировать факторы транскрипции Xwnt-8 или BMP-4. Gsc прямо подавляет экспрессию Xwnt-8, косвенно подавляя BMP-4.[12] Ингибирование Xwnt-8 и BMP-4 гарантирует, что может произойти нормальное переднее развитие, которое стимулируется организатором Spemann.
Экспрессия Gsc происходит дважды в процессе развития, сначала во время гаструляции, а затем во время органогенеза.[13] Gsc находится в высоких концентрациях в дорсальной мезодерме и энтодерма во время гаструляции. Более поздняя экспрессия Gsc ограничена областью головы. У Xenopus клетки, экспрессирующие Gsc, становятся энтодермой глотки, мезодермой головы, брюшной скелетной тканью головы и нотокордом.[14]
Мутации
Мутация в гене GSC вызывает низкий рост, атрезию слухового прохода, гипоплазию нижней челюсти и аномалии скелета (SAMS). Ранее считалось, что САМС является аутосомно-рецессивным заболеванием, но исследования с молекулярным кариотипированием и секвенированием всего экзома (WES) показали обратное.[15]
Мутации в гене Gsc могут приводить к специфическим фенотипам в результате второй экспрессии гена Gsc во время органогенеза. Нокаут-модели гена у мышей выражают дефекты языка, носовой полости, носовых ямок, внутреннего уха и наружного слухового прохода.[16] Новорожденные мыши, рожденные с этой мутацией, умирают в течение 24 часов из-за осложнений с дыханием и сосанием молока в результате черепно-лицевых аномалий, вызванных мутацией. Мутации гена Gsc у людей могут привести к состоянию, известному как синдром САМС, характеризующемуся низким ростом, атрезией слухового прохода, гипоплазией нижней челюсти и аномалиями скелета.[15][17]
Роль в развитии рака
Благодаря своей роли фактор транскрипции В миграции клеток во время эмбрионального развития GSC рассматривается как потенциальный игрок в развитии рака и метастазировании, поскольку эмбриональное развитие и развитие рака имеют сходные характеристики. GSC, наряду с другими факторами транскрипции, такими как Крутить, FOXC2, и Улитка, индуцируют эпителиальный мезенхимальный переходы, регулируя белки клеточной адгезии E-кадгерин, α-катенин и экспрессия γ-катенина в эпителиальных клетках.[18] Исследования показали, что в высокометастатических раковых клетках яичников, легких, молочной железы и других раковых клетках GSC высоко экспрессируется на ранних стадиях прогрессирования опухоли.[19] Кроме того, высокие уровни экспрессии GSC в раковых клетках коррелируют с плохой выживаемостью и, таким образом, могут использоваться в качестве инструмента прогноза.[20] Высокая экспрессия GSC также коррелирует с химической устойчивостью рака. Следовательно, GSC «готовит клетки к проявлению агрессивных фенотипов».[19]»И« могут быть наиболее потенциальными биомаркерами лекарственного ответа и плохого прогноза.[20]”
Рекомендации
- ^ а б c ГРЧ38: Ансамбль выпуск 89: ENSG00000133937 - Ансамбль, Май 2017
- ^ а б c GRCm38: выпуск Ensembl 89: ENSMUSG00000021095 - Ансамбль, Май 2017
- ^ "Справочник человека по PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ "Ссылка на Mouse PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ Блюм М., Де Робертис Э.М., Коджис Т., Хайнцманн С., Клисак И., Гейссерт Д., Спаркс Р.С. (май 1994 г.). «Молекулярное клонирование гена гомеобокса человека goosecoid (GSC) и картирование гена на хромосоме человека 14q32.1». Геномика. 21 (2): 388–93. Дои:10.1006 / geno.1994.1281. PMID 7916327.
- ^ а б "Entrez Gene: GSC goosecoid".
- ^ Izpisúa-Belmonte JC, De Robertis EM, Storey KG, Stern CD (август 1993 г.). «Гуськоид ген гомеобокса и происхождение клеток-организаторов в ранней бластодерме цыплят». Клетка. 74 (4): 645–59. Дои:10.1016 / 0092-8674 (93) 90512-о. PMID 7916659.
- ^ Нирс К., Келлер Р., Чо К.В., Де Робертис Э.М. (1993). "Ген гомеобокса гусекоид контролирует миграцию клеток в Xenopus эмбрионы ". Клетка. 72 (4): 491–503. Дои:10.1016/0092-8674(93)90069-3. PMID 8095000.
- ^ Steinbeisser H, Fainsod A, Niehrs C., Sasai Y, De Robertis EM (ноябрь 1995 г.). «Роль gsc и BMP-4 в формировании дорсально-вентрального паттерна маргинальной зоны у Xenopus: исследование потери функции с использованием антисмысловой РНК». Журнал EMBO. 14 (21): 5230–43. Дои:10.1002 / j.1460-2075.1995.tb00208.x. ЧВК 394633. PMID 7489713.
- ^ Ривера-Перес Дж. А., Малло М., Гендрон-Магуайр М., Гридли Т., Берингер Р. Р. (сентябрь 1995 г.). «Гуськоид не является важным компонентом организатора гаструлы мыши, но необходим для черепно-лицевого развития и развития ребер». Разработка. 121 (9): 3005–12. PMID 7555726.
- ^ Гориели А., Стелла М., Коффинье С., Кесслер Д., Майлос С., Дессейн С., Десплан С. (май 1996 г.). «Функциональный гомолог гусекоида у дрозофилы». Разработка. 122 (5): 1641–50. PMID 8625850.
- ^ Яо Дж, Кесслер Д.С. (август 2001 г.). «Goosecoid способствует деятельности главного организатора путем прямого подавления Xwnt8 в организаторе Спеманна». Разработка. 128 (15): 2975–87. PMID 11532920.
- ^ Ямада Дж., Мансури А., Торрес М., Стюарт Е. Т., Блюм М., Шульц М., Де Робертис Е. М., Грусс П. (сентябрь 1995 г.). «Нацеленная мутация гена мышиного гусекоида приводит к черепно-лицевым дефектам и неонатальной смерти». Разработка. 121 (9): 2917–22. PMID 7555718.
- ^ Де Робертис Э., Блюм М., Нирс С., Штайнбайсер Х. (апрель 1992 г.). «Индукция мезодермы и происхождение эмбриональной оси: гусекоид и организатор». Разработка. 116: 167–171.
- ^ а б Парри Д.А., Логан CV, Стегманн А.П., Абдельхамед З.А., Колдер А., Хан С., Бонтрон Д.Т., Клоуз В., Шеридан Э., Гали Н., Чадли А.Э., Добби А., Штумпел, CT, Джонсон, Калифорния (декабрь 2013 г.). "САМС, синдром низкого роста, атрезии слухового канала, гипоплазии нижней челюсти и скелетных аномалий - уникальная нейрокристопатия, вызванная мутациями при гусекоиде". Американский журнал генетики человека. 93 (6): 1135–42. Дои:10.1016 / j.ajhg.2013.10.027. ЧВК 3853132. PMID 24290375.
- ^ Ямада Г., Уэно К., Накамура С., Ханамур Ю., Ясуи К., Уэмура М., Эйзуру Ю., Мансури А., Блюм М., Сугимура К. (апрель 1997 г.). «Носовые и глоточные аномалии, вызванные мутацией гена гусекоидного гуся у мышей». Сообщения о биохимических и биофизических исследованиях. 233 (1): 161–5. Дои:10.1006 / bbrc.1997.6315. PMID 9144415.
- ^ Lemire EG, Hildes-Ripstein GE, Reed MH, Chudley AE (январь 1998 г.). «САМС: временно уникальный синдром множественных врожденных аномалий, состоящий из низкого роста, атрезии слухового прохода, гипоплазии нижней челюсти и аномалий скелета». Американский журнал медицинской генетики. 75 (3): 256–60. Дои:10.1002 / (sici) 1096-8628 (19980123) 75: 3 <256 :: aid-ajmg5> 3.0.co; 2-o. PMID 9475592.
- ^ Мани С.А., Ян Дж., Брукс М., Шванингер Дж., Чжоу А., Миура Н., Куток Дж. Л., Хартвелл К., Ричардсон А. Л., Вайнберг Р. А. (июнь 2007 г.). «Мезенхима Forkhead 1 (FOXC2) играет ключевую роль в метастазировании и связана с агрессивным базальным раком груди». Труды Национальной академии наук Соединенных Штатов Америки. 104 (24): 10069–74. Дои:10.1073 / pnas.0703900104. ЧВК 1891217. PMID 17537911.
- ^ а б Хартвелл К.А., Мюир Б., Райнхардт Ф., Карпентер А.Е., Сгрой округ Колумбия, Вайнберг Р.А. (декабрь 2006 г.). «Ген-организатор Spemann, Goosecoid, способствует метастазированию опухоли». Труды Национальной академии наук Соединенных Штатов Америки. 103 (50): 18969–74. Дои:10.1073 / pnas.0608636103. ЧВК 1748161. PMID 17142318.
- ^ а б Кан К.В., Ли MJ, Сон Дж.А., Чжон Дж.Й., Ким Ю.К., Ли Си, Ким Т.Х., Квак КБ, Ким О.Дж., Ан HJ (июль 2014 г.). «Избыточная экспрессия гомеобокса гусекоидного типа связана с химиорезистентностью и плохим прогнозом при карциноме яичников». Отчеты онкологии. 32 (1): 189–98. Дои:10.3892 / или 2014.3203. PMID 24858567.
дальнейшее чтение
- Schlade-Bartusiak K, Macintyre G, Zunich J, Cox DW (январь 2008 г.). «Ребенок с делецией (14) (q24.3q32.13) и слуховой нейропатией». Американский журнал медицинской генетики, часть A. 146A (1): 117–23. Дои:10.1002 / ajmg.a.32064. PMID 18074379.
- Хартвелл К.А., Мюир Б., Райнхардт Ф., Карпентер А.Е., Сгрой округ Колумбия, Вайнберг Р.А. (декабрь 2006 г.). «Ген-организатор Spemann, Goosecoid, способствует метастазированию опухоли». Труды Национальной академии наук Соединенных Штатов Америки. 103 (50): 18969–74. Дои:10.1073 / pnas.0608636103. ЧВК 1748161. PMID 17142318.
- Барриос-Родилес М., Браун К. Р., Оздамар Б., Бозе Р., Лю З., Донован Р. С., Синджо Ф., Лю Ю., Дембовы Дж., Тейлор И. В., Луга В., Прзулдж Н., Робинсон М., Сузуки Н., Хаяшизаки Ю., Юрисика И., Wrana JL (март 2005 г.). «Высокопроизводительное отображение динамической сигнальной сети в клетках млекопитающих». Наука. 307 (5715): 1621–5. Дои:10.1126 / science.1105776. PMID 15761153.
- Намчиу С.Дж., Фридман Р.Д., Марсден М.Д., Сараусад Л.М., Джейсони С.Л., Фурнье Р.Э. (март 2004 г.). «Последовательность организации и области прикрепления матрикса кластера генов ингибитора сериновой протеазы человека в 14q32.1». Геном млекопитающих. 15 (3): 162–78. Дои:10.1007 / s00335-003-2311-y. PMID 15014966.
- Foucher I, Montesinos ML, Volovitch M, Prochiantz A, Trembleau A (май 2003 г.). «Совместная регуляция промотора MAP1B с помощью HNF3beta / Foxa2 и Engrailed является результатом высококонсервативного механизма прямого взаимодействия гомеопротеинов и факторов транскрипции Fox». Разработка. 130 (9): 1867–76. Дои:10.1242 / dev.00414. PMID 12642491.
- Данилов В., Блюм М., Швайкерт А., Кампионе М., Штайнбайссер Н. (январь 1998 г.). «Отрицательная ауторегуляция гуцекоида, специфичного для организатора гомеобокса». Журнал биологической химии. 273 (1): 627–35. Дои:10.1074 / jbc.273.1.627. PMID 9417125.